Elektroniczna recepta transgraniczna. Science-fiction czy niedaleka rzeczywistość?
- dr Anna Gawrońska, ekspert ds. standardów GS1 w ochronie zdrowia
- Kategoria: Wieści z GS1

Z uwagi na coraz większą mobilność Europejczyków, liczne podróże i częste zmiany miejsca pobytu, kluczowego nowego wymiaru nabrało świadczenie usług medycznych w ujęciu transgranicznym, w tym możliwość wystawiania i realizacji recept przez pacjentów za granicą. Kwestie z tym związane są uregulowane prawnie i umożliwiają wystawianie recept w postaci papierowej. Wśród przedstawicieli branży ochrony zdrowia na poziomie Unii Europejskiej zarysowuje się dążenie do wypracowania rozwiązania w zakresie elektronizacji tej procedury.
Elektroniczna recepta kojarzona jest nadal jako symbol innowacji i nowoczesnych rozwiązań w obszarze ochrony zdrowia w Polsce. W związku z tym nie brakuje obaw i wątpliwości, związanych z przekonaniem co do braku gotowości do wprowadzenia takiego rozwiązania w Polsce, jak również skuteczności i efektywności jego funkcjonowania. Eksperci twierdzą, że obawy nie są w pełni uzasadnione, ponieważ apteki są wyposażone w sprzęt komputerowy i odpowiednie informatyczne programy apteczne. Wszystkie gabinety lekarskie, przychodnie i inne placówki nie tylko muszą posiadać komputery, ale także bezpieczne oraz stabilne łącze internetowe. Odpowiednie wyposażenie, jak również przeszkolenie lekarzy powinno mieć miejsce po to, aby wszystkie strony były odpowiednio przygotowane na realizację założeń elektronicznej recepty.
Wśród różnorodnych czynników technicznych, od których uzależnione jest skuteczne i efektywne funkcjonowanie elektronicznej recepty, kluczową rolę odgrywa również rejestr produktów leczniczych. Na podstawie tego rejestru osoba uprawniona do wystawienia recepty będzie tworzyła wykaz produktów leczniczych dla pacjenta. W Polsce referencyjny rejestr powstał w ramach tzw. projektu P2, czyli „Platformy udostępniania on-line przedsiębiorcom usług i zasobów cyfrowych rejestrów medycznych”, zrealizowanego przez Centrum Systemów Informacyjnych Ochrony Zdrowia (CSIOZ). Rejestr ten obejmuje produkty lecznicze dopuszczone do obrotu na terytorium Rzeczypospolitej Polskiej oraz produkty lecznicze wpisane do Wspólnotowego Rejestru Produktów Leczniczych.
Można zatem stwierdzić, że prędzej czy później zaistnieją w Polsce warunki do skutecznego i efektywnego wystawiania i realizacji recept w postaci elektronicznej. Czy jednak taka recepta – wystawiona w Polsce – będzie mogła być zrealizowana w innym kraju Unii Europejskiej przy sprzyjających uwarunkowaniach prawnych? Między innymi tak postawione pytanie stało się przedmiotem dyskusji wielu krajów UE. Mimo jednolitych dla krajów członkowskich regulacji prawnych, każdy z krajów charakteryzuje się własnym, bardzo często specyficznym, podejściem w zakresie uregulowań krajowych. Ma to z kolei wpływ na sposób opisu i identyfikacji produktów leczniczych przepisywanych pacjentom w ramach określonej farmakoterapii. Takie podejście niesie za sobą określone konsekwencje w postaci braku jednolitego dla UE słownika produktów leczniczych, który umożliwiałby skuteczną realizację elektronicznej recepty wystawionej w kraju innym niż kraj, w którym ta recepta została wystawiona.
Powodem trudności w zakresie realizacji recepty elektronicznej w ujęciu transgranicznym jest – oprócz braku jednolitego słownika produktów leczniczych – również różny sposób przepisywania leków. Istnieje możliwość przepisywania leków stosujących ich nazwę międzynarodową, chemiczną lub handlową. Przy czym należy pamiętać, że nazwy handlowe mogą różnić się w zależności od kraju. Ponadto, na terenie UE istnieją różne procedury rejestracji produktów leczniczych, różne sposoby dopuszczania produktów do obrotu, a co się z tym wiąże: różne metody kodowania danych o produktach. Brak jednolitego podejścia w zakresie identyfikacji produktów leczniczych jest również następstwem stosowania krajowych identyfikatorów i atrybutów leków, które rozumiane są tylko w państwie, w którym są stosowane. Dodatkowym utrudnieniem są także różnorodne podejścia w zakresie stosowania zamienników oraz rodzaju dostępności produktów leczniczych (leki OTC a leki Rp).
W związku z powyższym na poziomie unijnym coraz częściej obserwuje się trendy standaryzacyjne, zmierzające do ujednolicenia sposobu gromadzenia i wymiany danych o produktach leczniczych. Działania i inicjatywy podejmowane na poziomie Unii Europejskiej w wyraźny sposób odzwierciedlają sygnalizowaną przez przedstawicieli ochrony zdrowia konieczność harmonizacji i standaryzacji określonych rozwiązań i sposobów przebiegu wybranych procesów. Konieczność ta jest rezultatem większej mobilności obywateli UE i dążeniem do jak największego poziomu obsługi pacjentów w kontekście świadczenia usług medycznych w ujęciu transgranicznym. Celem takich działań jest zapewnienie bezpieczeństwa farmakoterapii, a co za tym idzie bezpieczeństwa pacjentów.
Wypracowanie koncepcji mechanizmu sprzyjającego realizacji elektronicznej recepty transgranicznej było ideą, która przyświecała zainicjowanemu w 2014 roku projektowi o nazwie OpenMedicine. W projekcie uczestniczyło 8 partnerów z UE, przy wsparciu bardzo licznej grupy ekspertów zewnętrznych. Należą do niej przedstawiciele takich instytucji, jak Światowa Organizacja Zdrowia (WHO, ang. World Health Organization), Europejska Agencja Leków (EMA, ang. European Medicines Agency) czy amerykański Urząd ds. Leków i Żywności (FDA, ang. Food and Drug Administration). W rezultacie realizacji prac, wypracowano koncepcję wspólnego modelu danych, jak również wspólnej nomenklatury.
Punkt wyjścia dla opracowanej koncepcji stanowił zestaw pięciu międzynarodowych standardów ISO w zakresie zharmonizowanego podejścia na rzecz identyfikacji i opisu produktów leczniczych, tzw. ISO IDMP (ang. Identification of Medicinal Products). Normy te EN ISO 11238, EN ISO 11239, EN ISO 11240, EN ISO 11615, EN ISO 11616 stanowią podstawę unikalnej identyfikacji produktów leczniczych, dając organom odpowiedzialnym za nadzór nad tymi produktami narzędzie wykorzystywane w procesie rozwoju, rejestracji i zarządzania cyklem życia produktów leczniczych, jak również monitorowania działań niepożądanych i zarządzaniem ryzykiem. Część integralną przedmiotowych norm stanowią specyfikacje w zakresie wymiany danych. Warto podkreślić, że normy te odwołują się i bazują na określonych standardach i rozwiązaniach w przedmiotowych obszarach, np. jednostek miary (SI), standardu wymiany danych medycznych (HL7), czy globalnych standardów w zakresie identyfikacji (GS1).
Zgodnie z Rozporządzeniem Wykonawczym Komisji (UE) NR 520/2012 z dnia 19 czerwca 2012 r. w sprawie działań związanych z nadzorem nad bezpieczeństwem farmakoterapii, o których mowa w rozporządzeniu (WE) nr 726/2004 Parlamentu Europejskiego i Rady i w dyrektywie 2001/83/WE Parlamentu Europejskiego i Rady w stosunku do branży farmaceutycznej sformułowano wymóg prawny co do posługiwania się terminologią zgodną z normami ISO. Przedmiotowe normy zostały wybrane nie tylko dlatego, że standaryzują podejście w zakresie unikalnej i zharmonizowanej identyfikacji produktów leczniczych dla różnorodnych celów i uwspólniają zasady opisu i wymiany danych o lekach. Będą one stanowiły fundament bazy danych produktów leczniczych, tworzonej przez Europejską Agencję Leków na rzecz monitorowania bezpieczeństwa leków i zgłaszania ich działań niepożądanych.
Z praktycznego punktu widzenia każdemu produktowi leczniczemu nadane zostaną określone i uzgodnione identyfikatory, umożliwiające jednoznaczną identyfikację takiego leku na różnych poziomach, tj.:
- identyfikator produktu farmaceutycznego: substancja czynna, postać, dawka (ang. pharmaceutical product identifier, w skrócie PhPID),
- identyfikator produktu leczniczego: podmiot odpowiedzialny, substancja czynna, nazwa handlowa, postać, dawka (ang. medicinal product identifier, w skrócie MPID),
- identyfikator produktu leczniczego w określonej formie opakowaniowej: podmiot odpowiedzialny, substancja czynna, nazwa handlowa, postać, dawka, liczba sztuk w opakowaniu (ang. packaging identifier, w skrócie PCID).
Dzięki takiemu ujednoliconemu podejściu możliwa będzie realizacja recepty w postaci elektronicznej transgranicznie według następującego schematu:
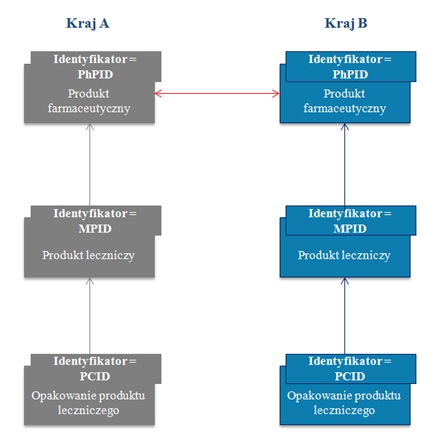
Wspólnym poziomem identyfikacji na poziomie UE będzie tzw. PhPID. Należy pamiętać, że proponowana koncepcja będzie możliwa do realizacji w momencie, kiedy wszystkie państwa członkowskie zaimplementują koncepcję ISO IDMP do krajowych słowników leków. Ponadto, bazy te będą musiały komunikować się z tworzoną przez EMA bazą europejską. Przewiduje się, że początek implementacji nie nastąpi wcześniej niż w 2018 roku. Od tej daty nie tylko wygoda podróżujących pacjentów, ale i ich bezpieczeństwo powinny wzrosnąć.

